Arbeitsgruppe Zelluläre Adhäsion
Die Arbeitsgruppe untersucht die zelluläre Adhäsion und ihre Bedeutung für die Entwicklung bioaktiver Biomaterialien. Die erfolgreiche Integration von Biomaterialien in biologische Systeme wird maßgeblich durch ihre Fähigkeit bestimmt, zelluläre Adhäsionsprozesse adäquat zu ermöglichen. Die Wechselwirkungen zwischen dem Biosystem und der Oberfläche des Biomaterials sind entscheidend für die Biokompatibilität, also die Fähigkeit keine unerwünschten zellulären Reaktionen hervorzurufen, und für die Bioaktivität, welche die Induktion gewebespezifischer Regenerationsprozesse umfasst. Diese Interaktionen an der Grenzfläche zwischen Material und biologischem Gewebe bestimmen wesentlich die funktionelle Leistungsfähigkeit und Verträglichkeit des eingesetzten Biomaterials.
Die physiko-chemischen Eigenschaften einer Biomaterialoberfläche spielen eine zentrale Rolle bei der Steuerung zellulärer Reaktionen. Nach der Einbringung eines Biomaterials in den Körper kommt es zunächst zur Adsorption von Proteinen auf dessen Oberfläche. Diese Proteine bilden eine interaktive Schicht, die als Vermittler für die nachfolgende Zelladhäsion fungiert. Die mit der Proteinschicht in Kontakt tretenden Zellen beginnen sich auf der Oberfläche auszubreiten, ein Vorgang, der als "Spreading" bezeichnet wird und entscheidend für die Integration des Biomaterials ist. Das Spreading wird maßgeblich durch die Umstrukturierung des Aktinzytoskeletts unterstützt. Dieses dynamische Netzwerk aus Proteinfilamenten erfüllt mehrere wichtige Funktionen: Es ermöglicht die strukturelle Anpassung der Zelle während des Spreadings, dient als Plattform für die intrazelluläre Signalübertragung und spielt eine Schlüsselrolle bei der Mechanotransduktion, also der Umwandlung mechanischer Reize in biochemische Signale. Die Wechselwirkungen zwischen Biomaterialoberfläche, adsorbierten Proteinen und adhärierenden Zellen bilden ein komplexes System, dessen Verständnis fundamental für die Entwicklung und Optimierung von Biomaterialien ist.
Die Zell-Biomaterial-Interaktion beeinflusst maßgeblich zelluläre Prozesse wie Adhäsion, Migration, Proliferation und Differenzierung. Eine optimierte Gestaltung dieser Interaktion ermöglicht es, Biomaterialien als effektive Hilfsmittel zur Geweberegeneration einzusetzen. Dabei ist das Verständnis der zugrundeliegenden zellulären Mechanismen von zentraler Bedeutung für die Entwicklung funktionaler Biomaterialien:
Zelluläre Reaktion auf Mikrostrukturen – ein Beitrag zur Optimierung von Implantatoberflächen
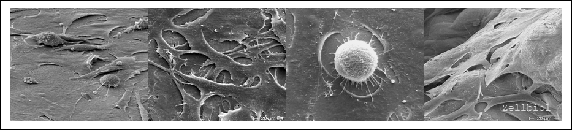
Im Rahmen des Graduiertenkollegs 1505 welisa konnte gezeigt werden, dass definierte Mikrostrukturen mit scharfen Kanten – wie Mikropfosten von 5?µm – in humanen Knochenzellen (Osteoblasten) ein phagozytoseähnliches Verhalten auslösen. Dieses Verhalten wird als ein aktiver Versuch der Zelle interpretiert, den Kontakt zur Oberfläche anzupassen. Scharfkantige Mikrostrukturen führen zu lokal erhöhtem mechanischem Stress an der Zellmembran. Um diesen zu kompensieren, passt die Zelle aktiv ihre Morphologie an: sie „umschließt“ die Mikrostruktur, um die Pfosten zu beseitigen und so die zelluläre Adhäsionsfläche zu vergrößern. Diese Erkenntnisse leisten einen wichtigen Beitrag zum Verständnis zellulärer Reaktionen auf Oberflächentopografien und können gezielt zur Entwicklung optimierter Implantatmaterialien genutzt werden, die eine bessere Zellintegration und Gewebeverträglichkeit fördern. [Link: Staehlke S et al. Biomaterials. 2015; 46: 48-57; doi:10.1016/j.biomaterials.2014.12.016]. [Link: Moerke C et al., J Mater Sci Mater Med. 2017, 28, 171; doi: 10.1007/s10856-017-5982-8].
Einfluss moderat positiv geladener Biomaterialoberflächen auf zelluläre Funktionen
Innerhalb der ersten Förderperiode des Sonderforschungsbereichs (SFB) 1270/2 ELAINE wurden „zellfreundliche Biomaterialschichten“ systematisch charakterisiert. Dabei zeigte sich, dass Materialoberflächen mit einer moderat positiven Oberflächenladung (Zetapotential: +1 bis +10 mV) das Zellverhalten positiv beeinflussten. Insbesondere förderten diese Oberflächen das Zellspreading, die Kalziumionen-Mobilisierung, die Membranintegrität und die Proliferation. Diese Ergebnisse unterstreichen die Bedeutung der Oberflächenladung als steuerbaren Parameter zur gezielten Modulation zellulärer Antworten und liefern eine wichtige Grundlage für die Entwicklung biofunktionaler Implantatmaterialien. [Link: Gruening M et al., Frontiers in Bioengineering and Biotechnology 2020, 8, 1016; doi: 10.3389/fbioe.2020.01016].
Chemische Modifikation von Biomaterialoberflächen durch Aminogruppen zur Verbesserung der Zelladhäsion
Das deutsch-französische Projekt AMINOCOAT (DFG-ANR) lieferte wichtige Erkenntnisse zur Rolle von Aminogruppen auf Biomaterialoberflächen, zur Verbesserung der Zelladhäsion und Förderung zellulärer Reaktionen. Die Studie zeigte, dass sowohl die Präsenz als auch die Dichte dieser Aminogruppen von entscheidender Bedeutung für die Verbesserung der Zelladhäsion sind und somit eine zentrale Rolle bei der Entwicklung und Optimierung bioaktiver Knochenimplantate spielen. [Link: Seemann S et al., Molecules 2023, 28, 6505; doi.org/10.3390/molecules28186505].
Der Forschungsfokus dieser Arbeitsgruppe konzentriert sich auf die detaillierte Untersuchung zellulärer Mechanismen an der Grenzfläche zu Biomaterialien. Ein besonderer Schwerpunkt liegt dabei auf der Analyse der Zell-Biomaterial-Interaktion unter Berücksichtigung spezifischer Materialmodifikationen. Diese umfassen:
- Topographische Modifikationen (Mikro- und Nano-strukturierte Oberflächen)
- Chemische Modifikationen (Amino- oder Methylgruppen)
Durch die systematische Erforschung dieser Interaktionen soll ein tiefgreifendes Verständnis der zellulären Reaktionen auf verschiedene Biomaterialeigenschaften gewonnen werden. Dieses Wissen ist fundamental für die Entwicklung innovativer biomedizinischer Materialien und Implantate, die gezielt zelluläre Funktionen steuern und eine optimale Gewebeintegration fördern können.
- Strukturelle und funktionelle Zellantworten
- Zelluläre Vitalität, Proliferation, Zellwachstum, Migration und Differenzierung
- Mikroskopische Analyse der Organisation subzellulärer Strukturen wie Adhäsionskontakte (Integrin, Vinkulin) und Zytoskelettkomponenten (Aktin, Tubulin)
- Zelluläre Interaktion mit der Oberfläche
- Zellmorphologie und Spreading
- Integrin-vermittelte Adhäsion der Zellen
- Zelluläre Signalantworten und Stressmechanismen
- Mechano- und Signaltransduktion, u.a. Phosphorylierung von Signalproteinen und intrazelluläres Kalziumionen (Ca2+)-Signaling
- Zellulärer Stress über Nachweis reaktiver Sauerstoffspezies (ROS), ATP/ADP-Assay
Kooperationspartner, extern:

Leibniz-Institut für Plasmaforschung und Technologie e. V. (INP)
Greifswald, D
www.inp-greifswald.de
Prof. Dr. Klaus-Dieter Weltmann,
Prof. Dr. Thomas von Woedtke,
Dr. Frank Hempel

Institut de Sciences des Materiaux de Mulhouse (IS2M)
Frankreich
www.is2m.uha.fr
Dr. Karine Anselme

INNOVENT e.V.
Jena, D
www.innovent-jena.de
Sabrina Hauspurg M.Eng.

Klinik und Poliklinik für Mund-Kiefer-Gesichtschirurgie/Plastische Operationen
Universitätsmedizin Greifswald
Aktuelles
SFB ELAINE
Sonderforschungsbereich 1270
"ELektrisch Aktive ImplaNtatE - ELAINE"
an der Universität Rostock
wird bis 2029 verlängert.
⇒ Medieninformation vom 24.11.2025
CAPIRO
3 Jahres-Projekt zu Plasma & ionisierender Strahlung, gefördert von der Deutschen Krebshilfe.
⇒ Pressemitteilung vom 05.12.2025
SYLOBIO



